ANSM - Mis à jour le : 04/05/2020
OLIMEL N9E, émulsion pour perfusion Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre infirmier/ère.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que OLIMEL N9E, émulsion pour perfusion et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser OLIMEL N9E, émulsion pour perfusion ?
3. Comment utiliser OLIMEL N9E, émulsion pour perfusion ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver OLIMEL N9E, émulsion pour perfusion ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE OLIMEL N9E, émulsion pour perfusion ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : SOLUTIONS POUR NUTRITION PARENTERALE / ASSOCIATIONS.
Code ATC : B05BA10
OLIMEL N9E est une émulsion pour perfusion. Il se présente sous la forme d’une poche à 3 compartiments.
Un compartiment contient une solution de glucose avec du calcium, un second une émulsion lipidique et le troisième une solution d’acides aminés avec d'autres électrolytes.
OLIMEL N9E est destiné à alimenter des adultes et des enfants de plus de deux ans au moyen d'une tubulure veineuse lorsque le patient ne peut pas s'alimenter normalement par la bouche.
OLIMEL N9E doit être administré uniquement sous surveillance médicale.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER OLIMEL N9E, émulsion pour perfusion ?
N'utilisez jamais OLIMEL N9E, émulsion pour perfusion :
·Chez les nouveau-nés prématurés, les nourrissons et chez les enfants âgés de moins de 2 ans,
- Si vous êtes hypersensible (allergique) aux protéines d'œuf, de soja, d'arachide ou au maïs et aux produits à base de maïs (voir également la rubrique « Avertissements et précautions » ci-dessous) ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6,
- Si votre corps réagit mal à certains acides aminés,
·Si votre sang contient un taux particulièrement élevé de graisses,
·Si vous souffrez d'hyperglycémie (trop de sucre dans le sang),
·Si vous avez une quantité anormalement élevée de l'un des électrolytes (sodium, potassium, magnésium, calcium et/ou phosphore) dans le sang.
Dans tous les cas, votre médecin décidera de vous prescrire ce médicament en tenant compte de critères tels que votre âge, votre poids et votre état de santé, et éventuellement des résultats des examens réalisés.
Avertissements et précautionsAdressez-vous à votre médecin ou à votre infirmier/ère avant qu’OLIMEL N9E ne vous soit administré.
Si vous recevez des solutions de nutrition parentérale totale (NPT) trop rapidement, vous avez un risque de lésion ou de décès.
La perfusion doit être immédiatement arrêtée en cas d’apparition de signes anormaux ou de symptômes d'une réaction allergique (tels que sueurs, fièvre, frissons, maux de tête, éruption cutanée ou difficultés à respirer).
Ce médicament contient des phospholipides d'œuf et de l'huile de soja. Les protéines d'œuf et de soja peuvent entraîner des réactions d'hypersensibilité. Des réactions d'allergie croisée ont été observées entre les protéines de soja et d'arachide.
OLIMEL N9E contient du glucose dérivé du maïs, qui peut provoquer des réactions d’hypersensibilité si vous êtes allergique au maïs ou aux produits à base de maïs (voir rubrique « N'utilisez jamais OLIMEL N9E, émulsion pour perfusion : » ci-dessus).
Des difficultés à respirer peuvent également être le signe que de petites particules se sont formées, bloquant ainsi les vaisseaux sanguins pulmonaires (précipités vasculaires pulmonaires). Si vous éprouvez des difficultés à respirer, informez-en votre médecin ou votre infirmier/ère. Ils décideront des actions à entreprendre.
L’antibiotique appelé ceftriaxone ne doit pas être mélangé ou administré simultanément avec des solutions contenant du calcium (comme OLIMEL N9E) qui vous sont administrées par une perfusion goutte-à-goutte dans une veine.
Ces médicaments ne doivent pas vous être administrés ensemble, même par une ligne de perfusion différente ou un site de perfusion différent.
Cependant, vous pouvez recevoir OLIMEL N9E et de la ceftriaxone séquentiellement, l’un après l’autre, si des lignes de perfusion sur des sites de perfusion différents sont utilisées ou si les lignes de perfusion sont remplacées, ou encore si elles ont été minutieusement rincées avec une solution de sérum physiologique entre les perfusions afin d’éviter toute précipitation (formation de particules de sel de ceftriaxone-calcium).
Certains médicaments et maladies peuvent augmenter le risque d’apparition d’une infection ou d’une septicémie (présence de bactéries dans le sang). Il existe un risque particulièrement élevé d'infection ou de septicémie lorsqu'une tubulure (cathéter intraveineux) est placée dans une veine. Votre médecin vous examinera attentivement pour détecter tout signe d'infection. Les patients nécessitant une nutrition parentérale (par le biais d'une tubulure placée dans une veine) sont plus susceptibles de développer une infection à cause de leurs pathologies. L'utilisation de techniques aseptiques ("sans germes") lors de la mise en place et de l'entretien du cathéter et lors de la préparation de la formulation nutritionnelle (NPT) peut réduire le risque d'infection.
Si vous êtes sévèrement dénutri au point d'avoir besoin de recevoir une alimentation par une veine, votre médecin doit débuter le traitement lentement. Votre médecin doit aussi vous surveiller attentivement lorsque vous recevez ce produit, afin d'empêcher des modifications soudaines de vos taux de fluides, de vitamines, d’électrolytes et de minéraux.
L’équilibre en eau et en sel dans votre corps ainsi que les perturbations du métabolisme seront corrigés avant de débuter la perfusion. Votre médecin surveillera votre état pendant toute la durée du traitement et pourra modifier la posologie ou prescrire des nutriments supplémentaires, notamment des vitamines, des électrolytes et des oligo-éléments, si cela est nécessaire.
Des troubles du foie, notamment des problèmes d'élimination de la bile (cholestase), de stockage de graisse (stéatose hépatique), de fibrose pouvant conduire à une insuffisance hépatique, ainsi que de cholécystite et de cholélithiase ont été rapportés chez des patients prenant un traitement nutritionnel par voie intraveineuse. Il se peut que la cause de ces troubles soit due à plusieurs facteurs et peut différer d’un patient à l’autre. Si vous souffrez de symptômes tels que des nausées, vomissements, douleurs abdominales, jaunissement de la peau ou du blanc des yeux, consultez votre médecin afin de permettre l'identification de facteurs causatifs et contributifs possibles ainsi que de mesures thérapeutiques et préventives possibles.
Votre médecin doit être informé si :
·Vous souffrez d’un problème rénal sévère. Vous devez aussi avertir votre médecin si vous êtes sous dialyse (rein artificiel) ou si vous avez un autre type de traitement de purification du sang.
·Vous souffrez d’un problème hépatique sévère.
·Vous avez des problèmes de coagulation du sang.
·Vos glandes surrénales ne fonctionnent pas correctement (insuffisance surrénalienne). Les glandes surrénales sont des glandes triangulaires situées au-dessus des reins.
·Vous souffrez de défaillance cardiaque.
·Vous avez une maladie des poumons.
·De l'eau s'accumule dans votre organisme (hyperhydratation).
·Votre organisme manque d'eau (déshydratation).
·Vous présentez une glycémie élevée (diabète) non contrôlée.
·Vous présentez une crise cardiaque ou un choc dû à une défaillance cardiaque soudaine.
·Vous souffrez d'une acidose métabolique grave (sang trop acide).
·Vous souffrez d'une infection généralisée (septicémie).
·Vous êtes dans le coma.
Pour contrôler l'efficacité et la sécurité de l'administration, votre médecin effectuera des examens cliniques et de laboratoire pendant que vous recevez ce médicament. Si vous avez reçu ce médicament sur plusieurs semaines, votre sang sera contrôlé régulièrement.
Une capacité réduite de l'organisme à éliminer les graisses contenues dans ce médicament peut entraîner un "syndrome de surcharge graisseuse" (voir rubrique 4 – Quels sont les effets indésirables éventuels ?).
Pendant la perfusion, si vous constatez une douleur, une sensation de brûlure ou un gonflement au site de perfusion ou une fuite de la perfusion, informez-en votre médecin ou votre infirmier/ère. L'administration sera immédiatement interrompue et de nouveau réalisée dans une autre veine.
Si votre glycémie devient trop élevée, votre médecin doit ajuster le débit d'administration d’OLIMEL N9E ou vous administrer un traitement de contrôle de la glycémie (insuline).
OLIMEL N9E peut seulement être administré par une tubulure (cathéter) dans une grosse veine de votre poitrine (veine centrale).
Enfants et adolescents
Si votre enfant est âgé de moins de 18 ans, une attention particulière sera portée pour qu’il/elle reçoive une dose correcte. De plus grandes précautions seront également prises en raison de la sensibilité plus importante des enfants aux risques d’infection. Une supplémentation en vitamines et en oligo-éléments est toujours nécessaire. Des formules pédiatriques doivent être utilisées.
Autres médicaments et OLIMEL N9E, émulsion pour perfusion
Informez votre médecin si vous prenez ou utilisez, avez récemment pris ou utilisé ou pourriez prendre ou utiliser tout autre médicament.
La prise concomitante d'autres médicaments n'est généralement pas contre-indiquée. Si vous prenez d'autres médicaments, avec ou sans prescription médicale, vous devez prévenir votre médecin à l'avance afin qu'il vérifie leur compatibilité.
Veuillez informer votre médecin si vous prenez ou recevez l'un des médicaments suivants :
- Insuline
·Héparine
OLIMEL N9E ne doit pas être administré simultanément avec du sang par la même tubulure de perfusion.
OLIMEL N9E contient du calcium. Il ne doit pas être administré en même temps ou par la même tubulure que l'antibiotique ceftriaxone en raison du risque de formation de particules. Si le même dispositif est utilisé pour vous administrer successivement ces médicaments, il doit être minutieusement rincé.
En raison du risque de précipitation, OLIMEL N9E ne doit pas être administré par la même ligne de perfusion que l’antibiotique ampicilline ou l’antiépileptique fosphénytoïne ni mélangé à ces deux produits.
Les huiles d'olive et de soja présentes dans OLIMEL N9E contiennent de la vitamine K. Cela n'influence normalement pas l’action des médicaments fluidifiant le sang (anticoagulants) tels que la coumarine. Néanmoins, si vous prenez des anticoagulants, vous devez en avertir votre médecin.
Les lipides contenus dans cette émulsion peuvent interférer avec les résultats de certains examens de laboratoire si le prélèvement sanguin a été réalisé avant l'élimination des lipides de votre circulation sanguine (ceux-ci sont normalement éliminés après 5 à 6 heures sans apport de lipides).
OLIMEL N9E contient du potassium. Il convient d'être particulièrement prudent chez les patients sous diurétiques, inhibiteurs de l’angiotensine (IEC) ou antagonistes du récepteur de l'angiotensine II (médicaments pour l'hypertension) ou immunosuppresseurs. Ces types de médicaments peuvent augmenter les taux de potassium dans votre sang.
OLIMEL N9E, émulsion pour perfusion avec des aliments, boissons et de l’alcoolSans objet.
Grossesse et allaitementSi vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant que vous receviez ce médicament.
Il n'y a pas d'expériences adéquates concernant l'utilisation d'OLIMEL N9E chez les femmes enceintes ou allaitantes. OLIMEL N9E peut être envisagé pendant la grossesse et l'allaitement, si cela est nécessaire. OLIMEL N9E ne doit être administré aux femmes enceintes ou allaitantes qu'après examen attentif.
Conduite de véhicules et utilisation de machinesSans objet.
OLIMEL N9E, émulsion pour perfusion contientSans objet.
3. COMMENT UTILISER OLIMEL N9E, émulsion pour perfusion ?
OLIMEL N9E doit être uniquement administré aux adultes et aux enfants âgés de plus de deux ans.
C'est une émulsion pour perfusion à administrer par une tubulure (cathéter) dans une grosse veine de votre poitrine.
OLIMEL N9E doit être à température ambiante avant utilisation.
OLIMEL N9E est seulement à usage unique.
La perfusion d’une poche dure généralement entre 12 et 24 heures.
Posologie - Adultes
Votre médecin vous précisera un débit de perfusion adapté à vos besoins et à votre état clinique.
La prescription peut être prolongée aussi longtemps que vous en avez besoin, selon votre état clinique.
Utilisation chez les enfants et les adolescentsPosologie - Enfants de plus de deux ans et adolescents
Le médecin déterminera la dose et la durée du traitement. Ceci dépendra de l'âge, du poids, de la taille, de l'état de santé, et de la capacité de l’organisme à dégrader et utiliser les composants d’OLIMEL N9E.
Si vous avez reçu plus d'OLIMEL N9E, émulsion pour perfusion que vous n'auriez dû
Si la dose qui vous a été donnée est trop élevée ou la perfusion trop rapide, les acides aminés risquent de rendre votre sang trop acide et des signes d'hypervolémie (augmentation du volume du sang circulant) peuvent être observés. Vos taux de glucose dans le sang et l'urine peuvent augmenter, un syndrome hyperosmolaire (augmentation de la viscosité du sang) peut apparaître et le contenu en lipides peut augmenter le taux de triglycérides dans votre sang. Une perfusion trop rapide ou l’administration d’un volume trop important d’OLIMEL N9E peut provoquer des nausées, vomissements, des frissons, des maux de tête, des bouffées de chaleur, une sudation excessive (hyperhidrose) et des perturbations électrolytiques. Dans ce cas, la perfusion doit être immédiatement interrompue.
Dans quelques cas sévères, votre médecin peut vous soumettre à une dialyse rénale à titre temporaire pour aider vos reins à éliminer l'excès de produit.
Pour éviter que ces situations ne surviennent, votre médecin surveillera régulièrement votre état et contrôlera vos paramètres sanguins.
Si vous oubliez d’utiliser OLIMEL N9E, émulsion pour perfusionSans objet.
Si vous arrêtez d’utiliser OLIMEL N9E, émulsion pour perfusionSans objet.
Si vous avez d’autres questions sur l'utilisation de ce médicament, demandez plus d’information à votre médecin.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Si vous constatez un changement dans votre état pendant ou après le traitement, informez-en immédiatement votre médecin ou le personnel infirmier.
Les contrôles que votre médecin effectue pendant le traitement devraient réduire le risque de survenue des effets indésirables.
Si des signes inhabituels ou des symptômes d'une réaction allergique se manifestent, tels que des sueurs, de la fièvre, des frissons, des maux de têtes, une éruption cutanée ou des difficultés à respirer, la perfusion doit être immédiatement arrêtée.
Les effets indésirables suivants ont été rapportés avec OLIMEL :
Fréquent : peut affecter jusqu’à 1 personne sur 10
- Fréquence cardiaque rapide (tachycardie)
- Appétit diminué
- Augmentation du taux de graisse dans le sang (hypertriglycéridémie)
- Douleur abdominale
- Diarrhée
- Nausée
- Pression artérielle augmentée (hypertension)
Fréquence indéterminée : ne peut être estimée sur la base des données disponibles
- Réaction d’hypersensibilité, notamment sueurs, fièvre, frissons, maux de tête, rash cutané (rash érythémateux, papuleux, pustuleux, maculeux, généralisé), démangeaisons, bouffée de chaleur, difficultés respiratoires.
·Fuite de la perfusion dans les tissus environnants (extravasation) pouvant entraîner les phénomènes suivants au niveau du site de perfusion : une douleur, une irritation, un gonflement/œdème, une rougeur (érythème)/chaleur, la mort des cellules tissulaires (nécrose de la peau) ou des ampoules/vésicules, une inflammation, un épaississement ou un tiraillement de la peau.
- Vomissements.
Les effets indésirables suivants ont été rapportés avec des produits de nutrition parentérale similaires:
Très rare : peut affecter jusqu’à 1 personne sur 10 000
·Réduction de la capacité à éliminer les lipides (syndrome de surcharge graisseuse) associée à une dégradation soudaine et abrupte de l'état de santé du patient. Les symptômes suivants de ce syndrome sont généralement réversibles après l'arrêt de la perfusion de l'émulsion lipidique :
oFièvre
oDiminution du nombre de globules rouges, ce qui peut augmenter la pâleur de la peau et entraîner une faiblesse ou un essoufflement (anémie)
oDiminution du nombre de globules blancs, ce qui peut accroître le risque d'infection (leucopénie)
oDiminution du nombre de plaquettes, ce qui peut accroître le risque de bleus et/ou de saignement (thrombopénie)
oTroubles de coagulation du sang
oTaux élevé de graisses dans le sang (hyperlipidémie)
oInfiltration graisseuse du foie (hépatomégalie)
oDétérioration de la fonction hépatique
oManifestations au niveau du système nerveux central (par exemple, coma)
Fréquence : indéterminée (ne peut être estimée sur la base des données disponibles)
·Réactions allergiques
·Résultats anormaux des examens sanguins de la fonction hépatique
·Problèmes d’élimination de la bile (cholestase)
·Augmentation de la taille du foie (hépatomégalie)
- Maladie du foie liée à la nutrition parentérale (voir la section "Mises en garde et précautions" à la section 2)
·Ictère (jaunisse)
·Baisse du nombre de plaquettes (thrombocytopénie)
·Hausse du taux d’azote dans le sang (azotémie)
·Enzymes hépatiques élevés
·Formation de petites particules pouvant entraîner le blocage des vaisseaux sanguins pulmonaires (précipités vasculaires pulmonaires) et provoquer ainsi une embolie pulmonaire d’origine vasculaire et des difficultés à respirer (détresse respiratoire).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance. Site internet : www.signalement-sante.gouv.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER OLIMEL N9E, émulsion pour perfusion ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la poche et la boîte (Mois/Année). La date de péremption fait référence au dernier jour de ce mois.
Ne pas congeler.
Conserver dans la surpoche.
Ne jetez aucun médicament au tout-à-l'égout ni avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l'environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient OLIMEL N9E, émulsion pour perfusion
Les substances actives de chaque poche de l'émulsion reconstituée sont :
· une solution d'acides aminés L à 14,2 % (correspondant à 14,2 g/100 mL) (alanine, arginine, glycine, histidine, isoleucine, leucine, lysine (sous forme d'acétate de lysine), méthionine, phénylalanine, proline, sérine, thréonine, tryptophane, tyrosine, valine, acide aspartique, acide glutamique) avec des électrolytes (sodium, potassium, magnésium, phosphate, acétate, chlorure),
· une émulsion lipidique à 20 % (correspondant à 20 g/100 mL) (huile d'olive raffinée et huile de soja raffinée)
· une solution de glucose à 27,5 % (correspondant à 27,5 g/100 mL) (sous forme de glucose monohydraté) avec du calcium.
Les autres composants sont :
|
Compartiment de l'émulsion lipidique |
Compartiment de la solution d'acides aminés avec électrolytes |
Compartiment de la solution de glucose avec calcium |
|
Phospholipides d'œuf purifié, glycérol, oléate de sodium, hydroxyde de sodium (pour ajustement du pH), eau pour préparations injectables |
Acide acétique glacial (pour ajustement du pH), eau pour préparations injectables |
Acide chlorhydrique (pour ajustement du pH), eau pour préparations injectables |
Qu’est-ce que OLIMEL N9E, émulsion pour perfusion et contenu de l’emballage extérieur
Aspect avant reconstitution :
- les solutions d'acides aminés et de glucose sont claires, incolores ou légèrement jaunes;
- l'émulsion lipidique est homogène et d'aspect laiteux.
Aspect après reconstitution : émulsion laiteuse et homogène.
La poche à trois compartiments est une poche en plastique multicouches. Le matériau de la couche (de contact) intérieure de la poche est compatible avec les constituants et les additifs autorisés.
Pour empêcher tout contact avec l'oxygène contenu dans l'air, la poche est conditionnée dans une surpoche étanche à l'oxygène avec un sachet absorbeur d'oxygène.
Présentations
Poche de 1 000 mL: 1 carton de 6 poches
Poche de 1 500 mL: 1 carton de 4 poches
Poche de 2 000 mL: 1 carton de 4 poches
1 poche de 1 000 mL, 1 500 mL et 2 000 mL
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
BAXTER S.A.SIMMEUBLE BERLIOZ
4 BIS RUE DE LA REDOUTE
78280 GUYANCOURT
Exploitant de l’autorisation de mise sur le marché
BAXTER S.A.SIMMEUBLE BERLIOZ
4 BIS RUE DE LA REDOUTE
78280 GUYANCOURT
BAXTER S.A.BOULEVARD RENE BRANQUART, 80
7860 LESSINES
BELGIQUE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.>[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé:
Classe pharmacothérapeutique : solutions pour nutrition parentérale / associations
Code ATC : B05BA10
A. COMPOSITION QUALITATIVE ET QUANTITATIVE
OLIMEL N9E, émulsion pour perfusion, se présente sous la forme d’une poche à 3 compartiments. Chaque poche contient une solution de glucose avec du calcium, une émulsion lipidique et une solution d’acides aminés avec d’autres électrolytes :
|
Contenus par poche |
|||
|
1000 mL |
1500 mL |
2000 mL |
|
|
Solution de glucose à 27,5 % (correspondant à 27,5 g/100 mL) |
400 mL |
600 mL |
800 mL |
|
Solution d’acides aminés à 14,2 % (correspondant à 14,2 g/100 mL) |
400 mL |
600 mL |
800 mL |
|
Émulsion lipidique à 20 % (correspondant à 20 g/100 mL) |
200 mL |
300 mL |
400 mL |
Composition de l’émulsion reconstituée, après mélange des contenus des 3 compartiments :
|
Substances actives |
1000 mL |
1500 mL |
2000 mL |
|||||
|
Huile d’olive raffinée + huile de soja raffinée a |
40,00 g |
60,00 g |
80,00 g |
|||||
|
Alanine |
8,24 g |
12,36 g |
16,48 g |
|||||
|
Arginine |
5,58 g |
8,37 g |
11,16 g |
|||||
|
Acide aspartique |
1,65 g |
2,47 g |
3,30 g |
|||||
|
Acide glutamique |
2,84 g |
4,27 g |
5,69 g |
|||||
|
Glycine |
3,95 g |
5,92 g |
7,90 g |
|||||
|
Histidine |
3,40 g |
5,09 g |
6,79 g |
|||||
|
Isoleucine |
2,84 g |
4,27 g |
5,69 g |
|||||
|
Leucine |
3,95 g |
5,92 g |
7,90 g |
|||||
|
Lysine (sous forme d’acétate de lysine) |
4,48 g (6,32 g) |
6,72 g (9,48 g) |
8,96 g (12,64 g) |
|||||
|
Méthionine |
2,84 g |
4,27 g |
5,69 g |
|||||
|
Phénylalanine |
3,95 g |
5,92 g |
7,90 g |
|||||
|
Proline |
3,40 g |
5,09 g |
6,79 g |
|||||
|
Sérine |
2,25 g |
3,37 g |
4,50 g |
|||||
|
Thréonine |
2,84 g |
4,27 g |
5,69 g |
|||||
|
Tryptophane |
0,95 g |
1,42 g |
1,90 g |
|||||
|
Tyrosine |
0,15 g |
0,22 g |
0,30 g |
|||||
|
Valine |
3,64 g |
5,47 g |
7,29 g |
|||||
|
Acétate de sodium, trihydraté |
1,50 g |
2,24 g |
2,99 g |
|||||
|
Glycérophosphate de sodium hydraté |
3,67 g |
5,51 g |
7,34 g |
|||||
|
Chlorure de potassium |
2,24 g |
3,35 g |
4,47 g |
|||||
|
Chlorure de magnésium, hexahydraté |
0,81 g |
1,22 g |
1,62 g |
|||||
|
Chlorure de calcium, dihydraté |
0,52 g |
0,77 g |
1,03 g |
|||||
|
Glucose (sous forme de glucose monohydraté) |
110,00 g (121,00 g) |
165,00 g (181,50 g) |
220,00 g (242,00 g) |
|||||
a : mélange d’huile d’olive raffinée (environ 80 %) et d’huile de soja raffinée (environ 20 %) correspondant à un ratio acides gras essentiels / acides gras totaux de 20 %.
Les autres composants sont :
|
Compartiment de l'émulsion lipidique |
Compartiment de la solution d'acides aminés avec électrolytes |
Compartiment de la solution de glucose avec calcium |
|
|
Phospholipides d'œuf purifié, glycérol, oléate de sodium, hydroxyde de sodium (pour ajustement du pH), eau pour préparations injectables |
Acide acétique glacial (pour ajustement du pH), eau pour préparations injectables |
Acide chlorhydrique (pour ajustement du pH), eau pour préparations injectables |
Apports nutritionnels de l’émulsion reconstituée pour chaque volume de poche :
|
1000 mL |
1500 mL |
2000 mL |
|
|
Lipides |
40 g |
60 g |
80 g |
|
Acides aminés |
56,9 g |
85,4 g |
113,9 g |
|
Azote |
9,0 g |
13,5 g |
18,0 g |
|
Glucose |
110,0 g |
165,0 g |
220,0 g |
|
Energie : |
|||
|
Calories totales env. |
1070 kcal |
1600 kcal |
2140 kcal |
|
Calories non protéiques |
840 kcal |
1260 kcal |
1680 kcal |
|
Calories glucidiques |
440 kcal |
660 kcal |
880 kcal |
|
Calories lipidiques a |
400 kcal |
600 kcal |
800 kcal |
|
Ratio calories non protéiques/azote |
93 kcal/g |
93 kcal/g |
93 kcal/g |
|
Ratio calories glucidiques/calories lipidiques |
52/48 |
52/48 |
52/48 |
|
Ratio calories lipidiques/calories totales |
37 % |
37 % |
37 % |
|
Electrolytes : |
|||
|
Sodium |
35,0 mmol |
52,5 mmol |
70,0 mmol |
|
Potassium |
30,0 mmol |
45,0 mmol |
60,0 mmol |
|
Magnésium |
4,0 mmol |
6,0 mmol |
8,0 mmol |
|
Calcium |
3,5 mmol |
5,3 mmol |
7,0 mmol |
|
Phosphate b |
15,0 mmol |
22,5 mmol |
30,0 mmol |
|
Acétate |
54 mmol |
80 mmol |
107 mmol |
|
Chlorure |
45 mmol |
68 mmol |
90 mmol |
|
pH |
6,4 |
6,4 |
6,4 |
|
Osmolarité |
1310 mosm/L |
1310 mosm/L |
1310 mosm/L |
a : inclut les calories des phospholipides d’œuf purifié
b : inclut les phosphates apportés par l’émulsion lipidique
B. POSOLOGIE ET MODE D'ADMINISTRATION
Posologie
L’utilisation d’OLIMEL N9E n’est pas recommandée chez les enfants âgés de moins de 2 ans, la composition et le volume n’étant pas appropriés (Voir rubriques 4.4, 5.1 et 5.2 du RCP).
La dose quotidienne maximale mentionnée ci-dessous ne doit pas être dépassée. En raison de la composition fixe de la poche multi-compartiments, il se peut qu’il ne soit pas possible de répondre à tous les besoins nutritionnels du patient en même temps. Il existe des situations cliniques où les patients ont besoin de quantité de nutriments différant de la composition de la poche. Dans ce cas, tout ajustement de volume (dose) doit tenir compte de l’effet que ce changement aura sur le dosage de tous les autres composants nutritionnels contenus dans OLIMEL N9E.
Chez les adultes
La posologie dépend de la dépense énergétique, de l’état clinique, du poids corporel du patient et de sa capacité à métaboliser les constituants d’OLIMEL N9E, ainsi que du supplément d’énergie ou de protéines administré par voie orale/entérale : le volume de la poche doit donc être choisi en conséquence.
Les besoins journaliers moyens sont :
·de 0,16 à 0,35 g d’azote par kg de poids corporel (1 à 2 g d’acides aminés/kg), selon l’état nutritionnel et le degré de stress catabolique du patient,
·de 20 à 40 kcal/kg,
·de 20 à 40 mL de liquide/kg ou de 1 à 1,5 mL par kcal consommée.
Pour OLIMEL N9E, la dose quotidienne maximale est déterminée par l’apport d’acides aminés, 35 mL/kg, correspondant à 2,0 g/kg d’acides aminés, 3,9 g/kg de glucose, 1,4 g/kg de lipides, 1,2 mmol/kg de sodium et 1,1 mmol/kg de potassium. Pour un patient de 70 kg, cela équivaut à 2450 mL d’OLIMEL N9E par jour, soit un apport de 140 g d’acides aminés, 270 g de glucose et 98 g de lipides (c’est-à-dire 2 058 kcal non protéiques et 2 622 kcal totales).
Le débit d’administration doit normalement être augmenté progressivement au cours de la première heure et ajusté ensuite en fonction de la dose à administrer, de l’apport volumique journalier et de la durée de la perfusion.
Pour OLIMEL N9E, le débit maximal de perfusion est de 1,8 mL/kg/heure, ce qui correspond à 0,10 g/kg/heure d’acides aminés, 0,19 g/kg/heure de glucose et 0,07 g/kg/heure de lipides.
Chez les enfants âgés de plus de 2 ans et les adolescents
Aucune étude n’a été réalisée dans la population pédiatrique.
La posologie dépend de la dépense énergétique, de l’état clinique, du poids corporel du patient et de sa capacité à métaboliser les constituants d’OLIMEL N9E, ainsi que du supplément d’énergie ou de protéines administré par voie orale/entérale : le volume de la poche doit donc être choisi en conséquence.
Par ailleurs, les besoins quotidiens en liquide, en azote et en énergie diminuent continuellement avec l’âge. Deux groupes, âgés de 2 à 11 ans et de 12 à 18 ans, sont pris en considération.
Pour OLIMEL N9E, dans le groupe âgé de 2 à 11 ans, la concentration en magnésium est le facteur limitant pour la dose journalière. Dans ce groupe d’âge, la concentration en glucose est le facteur limitant pour le débit par heure. Dans le groupe âgé de 12 à 18 ans, les concentrations en acides aminés et en magnésium sont le facteur limitant pour la dose journalière. Dans ce groupe d’âge, a concentration en acides aminés est le facteur limitant pour le débit par heure. Les apports obtenus sont affichés ci-dessous :
|
Composant |
de 2 à 11 ans |
de 12 à 18 ans |
||
|
Recommandée a |
Volume maximal d’OLIMEL N9E |
Recommandée a |
Volume maximal d’OLIMEL N9E |
|
|
Dose journalière maximale |
||||
|
35 |
60 - 120 |
25 |
50-80 |
35 |
|
Acides aminés (g/kg/jour) |
1 - 2 (jusqu'à 2,5) |
1,4 |
1 - 2 |
2,0 |
|
Glucose (g/kg/jour) |
1,4 – 8,6 |
2,8 |
0,7 – 5,8 |
3,9 |
|
Lipides (g/kg/jour) |
0,5 - 3 |
1,0 |
0,5 - 2 (jusqu’à 3) |
1,4 |
|
Energie totale (kcal/kg/jour) |
30 - 75 |
26,8 |
20 - 55 |
37,5 |
|
Débit maximal par heure |
||||
|
OLIMEL N9E (mL/kg/h) |
3,3 |
2,1 |
||
|
Acides aminés (g/kg/h) |
0,20 |
0,19 |
0,12 |
0,12 |
|
Glucose (g/kg/h) |
0,36 |
0,36 |
0,24 |
0,23 |
|
Lipides (g/kg/h) |
0,13 |
0,13 |
0,13 |
0,08 |
a : valeurs recommandées par les recommandations ESPGHAN/ ESPEN/ ESPR 2018
Le débit d’administration doit normalement être augmenté progressivement au cours de la première heure et ajusté ensuite en fonction de la dose à administrer, de l’apport volumique journalier et de la durée de la perfusion.
De manière générale, il est recommandé de débuter la perfusion chez les jeunes enfants par une dose journalière faible et de l’augmenter progressivement jusqu’à la dose maximale (voir ci-dessus).
Mode et durée d’administration
A usage unique.
Après ouverture de la poche, il est recommandé d’utiliser le contenu immédiatement et de ne pas le conserver pour une perfusion ultérieure.
Après reconstitution, le mélange est une émulsion homogène et d’aspect laiteux.
Pour les instructions concernant la préparation et la manipulation de l’émulsion pour perfusion, voir la rubrique 6.6 du RCP.
En raison de son osmolarité élevée, OLIMEL N9E ne peut être administré que par une veine centrale.
La durée de perfusion recommandée pour une poche de nutrition parentérale est comprise entre 12 et 24 heures.
La nutrition parentérale peut être poursuivie aussi longtemps que l’état clinique du patient l’exige.
C. INCOMPATIBILITES
Ne pas ajouter d’autres médicaments ou substances à tout composant de la poche ou à l’émulsion reconstituée sans vérifier préalablement leur compatibilité et la stabilité de la préparation obtenue (notamment, la stabilité de l’émulsion lipidique).
Des incompatibilités peuvent se produire, par exemple avec une acidité excessive (pH faible) ou une teneur non appropriée en cations divalents (Ca²+ et Mg2+), ce qui peut déstabiliser l’émulsion lipidique.
Comme avec tous les mélanges pour nutrition parentérale, il convient de tenir compte des taux de calcium et de phosphate. Un ajout excessif de calcium et de phosphate, en particulier sous forme de sels minéraux, peut entraîner la formation de précipités de phosphate de calcium.
OLIMEL N9E contient des ions calcium qui constituent un risque supplémentaire de coagulation en cas de précipitation dans du sang ou des composants sanguins contenant un agent conservateur/anticoagulant du type citrate.
La ceftriaxone ne doit pas être mélangée ni administrée simultanément par voie intraveineuse avec des solutions contenant du calcium, comme OLIMEL N9E, à l'aide de la même ligne de perfusion (ex., raccord en Y) en raison du risque de précipitation entre le sel de calcium et la ceftriaxone (voir rubriques 4.4 et 4.5 du RCP). La ceftriaxone et des solutions contenant du calcium peuvent être administrées séquentiellement, l’une après l’autre, si des lignes de perfusion sur des sites de perfusion différents sont utilisées ou si les lignes de perfusion sont remplacées, ou ont été minutieusement rincées entre les perfusions avec une solution de sérum physiologique afin d’éviter toute précipitation.
En raison du risque de précipitation, OLIMEL N9E ne doit pas être administré par la même ligne de perfusion que l’ampicilline ou la fosphénytoïne ni mélangé à ces deux produits.
Vérifier la compatibilité avec les solutions administrées simultanément par le même set d’administration, cathéter ou canule.
Ne pas administrer avant, pendant ou après une transfusion de sang en utilisant le même équipement en raison du risque de pseudo-agglutination.
D. PRECAUTIONS PARTICULIERES D’ELIMINATION ET DE MANIPULATION
Les étapes de préparation avant l’administration d’OLIMEL N9E sont présentées en figure 1 ci-après.
Pour ouvrir
·Retirer la surpoche de protection.
·Jeter l’absorbeur d’oxygène.
·Vérifier l’intégrité de la poche et des soudures non permanentes. Utiliser uniquement si la poche n’est pas endommagée, si les soudures non permanentes sont intactes (c'est-à-dire, sans mélange des contenus des trois compartiments) ; si la solution d’acides aminés et la solution de glucose sont limpides, incolores ou légèrement jaunes, et pratiquement exemptes de particules visibles ; et si l’émulsion lipidique est un liquide homogène d’aspect laiteux.
Mélange des solutions et de l’émulsion
·S’assurer que le produit est à température ambiante avant de rompre les soudures non permanentes.
·Enrouler manuellement la poche sur elle-même en commençant par le haut de la poche (côté œillet de suspension). Les soudures non permanentes disparaîtront du côté des embouts. Continuer d’enrouler la poche jusqu’à ce que les soudures soient ouvertes sur environ la moitié de leur longueur.
·Mélanger en retournant la poche au moins 3 fois.
·Après reconstitution, le mélange est une émulsion homogène et laiteuse.
Supplémentations
La capacité de la poche est suffisante pour permettre des supplémentations telles que des vitamines, des électrolytes et des oligo-éléments.
Toute supplémentation (y compris de vitamines) peut être faite dans le mélange reconstitué (après ouverture des soudures non permanentes et mélange du contenu des 3 compartiments).
Des vitamines peuvent également être ajoutées au compartiment de glucose avant reconstitution du mélange (avant rupture des soudures non permanentes et mélange des 3 compartiments).
Pour les supplémentations aux formules contenant des électrolytes, les électrolytes déjà présents dans la poche doivent être pris en compte.
Les supplémentations doivent se faire dans des conditions d’asepsie et par un personnel qualifié.
Des électrolytes peuvent être ajoutés à OLIMEL N9E, dans les limites du tableau ci-dessous :
|
Pour 1000 mL |
|||
|
Quantité présente |
Addition supplémentaire maximale |
Quantité totale maximale |
|
|
Sodium |
35 mmol |
115 mmol |
150 mmol |
|
Potassium |
30 mmol |
120 mmol |
150 mmol |
|
Magnésium |
4,0 mmol |
1,6 mmol |
5,6 mmol |
|
Calcium |
3,5 mmol |
1,5 (0,0 a) mmol |
5,0 (3,5 a) mmol |
|
Phosphate inorganique |
0 mmol |
3,0 mmol |
3,0 mmol |
|
Phosphate organique |
15 mmol b |
10 mmol |
25 mmol b |
a : valeur correspondant à l’ajout de phosphate inorganique
b : inclut les phosphates provenant de l’émulsion lipidique
Oligo-éléments et vitamines :
La stabilité a été démontrée avec les préparations de vitamines et d’oligo-éléments disponibles dans le commerce (contenant 1 mg de fer maximum).
La compatibilité pour d’autres supplémentations est disponible sur demande.
Pour effectuer une supplémentation :
·Respecter les conditions d’asepsie,
·Préparer le site d’injection de la poche,
·Ponctionner le site d’injection et injecter les additifs à l’aide d’une aiguille pour injection ou d’un dispositif de reconstitution,
·Mélanger le contenu de la poche et les additifs.
Préparation de la perfusion :
·Respecter les conditions d’asepsie.
·Suspendre la poche.
·Retirer le protecteur en plastique de l’embout d’administration.
·Insérer fermement le perforateur du set de perfusion dans l’embout d’administration.
Figure 1 : Étapes de préparation avant l'administration d’OLIMEL
|
1. |
|
2. |
|
3. |
|
|
|
Déchirer depuis le haut pour ouvrir la surpoche. |
Détacher le devant de la surpoche pour sortir la poche OLIMEL. Jeter la surpoche et le sachet absorbeur d'oxygène. |
Poser la poche à plat sur une surface horizontale et propre avec la poignée face à vous. |
||||
|
4. |
|
5. |
|
6. |
|
|
|
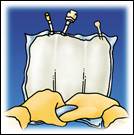
Soulever la zone de l'œillet pour retirer la solution de la partie supérieure de la poche. Rouler fermement la partie supérieure de la poche jusqu'à ce que les soudures pelables soient complètement ouvertes (environ sur la moitié de la longueur) |
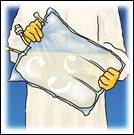
Mélanger en retournant la poche à l'envers au moins 3 fois. |
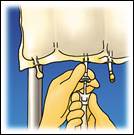
Suspendre la poche. Tourner et retirer le protecteur du site d'administration. Insérer fermement le perforateur du perfuseur |
||||
Administration :
A usage unique.
·Administrer uniquement le médicament après avoir rompu les soudures non permanentes entre les 3 compartiments et mélangé le contenu des 3 compartiments.
·Vérifier qu’il n’y a pas de séparation des phases dans l’émulsion finale à perfuser.
·Une fois la poche ouverte, utiliser immédiatement son contenu. Ne jamais conserver la poche ouverte pour une perfusion ultérieure. Ne pas reconnecter des poches partiellement utilisées.
·Ne pas connecter de poches en série afin d’éviter tout risque d’embolie gazeuse due à l’air contenu dans la première poche.
·Détruire tout produit restant, les déchets et accessoires nécessaires.
Extravasation
Le site d’insertion du cathéter doit être régulièrement contrôlé pour détecter les signes d'extravasation.
En cas d'extravasation, l'administration doit être interrompue immédiatement, tout en maintenant en place la canule ou le cathéter inséré pour une prise en charge immédiate du patient. Si possible, une aspiration doit être pratiquée à travers la canule/le cathéter inséré afin de réduire la quantité de liquide présent dans les tissus avant de retirer la canule/le cathéter.
Selon le produit extravasé (y compris le ou les produit(s) mélangés avec OLIMEL N9E, le cas échéant) et le stade/l'étendue des lésions éventuelles, des mesures spécifiques appropriées doivent être mises en place. Les options de prises en charges thérapeutiques peuvent inclure des interventions non pharmacologiques, pharmacologiques et/ou chirurgicales. En cas d'extravasation importante, un chirurgien plasticien doit être consulté dans les premières 72 heures.
Le site d'extravasation doit être contrôlé au moins toutes les 4 heures pendant les premières 24 heures, puis au moins une fois par jour.
La perfusion ne doit pas être à nouveau réalisée dans la même veine centrale.
Retrouvez la disponibilité de votre produit dans les pharmacies:
Adresse de livraison manquante
Pour trouver la pharmacie la plus proche de chez vous, veuillez ajouter votre adresse de livraison.